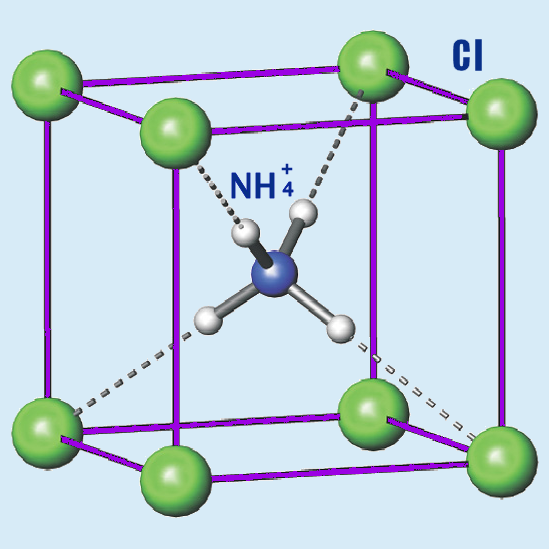
まとめ
- 水酸化カルシウムと混合して加熱することで、アンモニアを発生させる原料となる白色の結晶性粉末です。
- 塩酸とアンモニア水が中和して生成される「塩(えん)」の一種であり、その水溶液は酸性を示します。
- 塩化水素とアンモニアの気体が接触した際に生じる、白い煙のような微細な固体の正体です。
解説
塩化アンモニウムは、中学・高校理科においてアンモニアを発生させる際の代表的な試薬として登場します。水酸化カルシウムなどの強塩基と混ぜて加熱すると、弱塩基であるアンモニアが追い出される「弱塩基の遊離」という反応が起こります。発生したアンモニアは水に非常に溶けやすく、空気よりも軽いため、上方置換法で集めるのが一般的です。
また、この物質は強酸である塩酸と弱塩基であるアンモニア水の中和反応によって得られます。中和によってできた塩の水溶液が何性を示すかは、もとになった酸と塩基の強弱で決まります。塩化アンモニウムの場合は「強酸+弱塩基」の組み合わせであるため、水溶液中ではアンモニウムイオンの一部が加水分解して水素イオンを生じ、酸性を示します。これは、アンモニアと塩化水素の性質を比較する実験や、中和の仕組みを理解する上で非常に重要なポイントとなります。
塩化アンモニウムは、見た目は白い粉のような物質です。理科の実験では、この粉を別の薬と混ぜて温めることで、つんとしたにおいのする「アンモニア」という気体を発生させるために使われます。
また、アンモニアの気体と、塩酸(えんさん)から出てくる塩化水素(えんかすいそ)という気体がまざると、まるで白い煙(けむり)のようなものが出てきます。この煙の正体も、実は小さな粒になった塩化アンモニウムなのです。手品のような不思議な反応ですが、気体同士がくっついて固まりになるおもしろい現象です。
この粉は水によく溶け、電気を通しやすくする性質があるため、私たちがふだん使っている乾電池の中身としても役立っています。
北欧などでは、この塩化アンモニウムを味付けに使った「サルミアッキ」というお菓子があります。とても独特な味がすることで有名ですが、日本では理科の実験で使うイメージが強いので、お菓子に入っていると聞くとびっくりしてしまいますね。
記事の内容に誤りがありますか?
⚠️ 修正を提案する